


近日,安智因生物医学部负责人马懿博士,联合阜外医院实验诊断中心项目负责人杨航博士,以及华中科技大学同济医学院附属同济医院心血管内科的副主任医师李宗哲博士,在IF为29.983的欧洲心脏病杂志(EHJ)上共同发表了名为“A laboratory viewpoint of the consensus paper from the European Society of Cardiology regarding the utilization of the American College of Medical Genetics and Genomics pathogenic criteria for cardiomyopathy”的文章,针对此前欧洲心脏病学会(ESC)发表的关于心肌病遗传变异的解读及可干预性的立场声明中一些可能引起误会的美国医学遗传学与基因组学学会(ACMG)解读规则从临床实验室的角度进行讨论。
前言
目前,心血管病领域的诸多指南和共识都承认基因检测在遗传性心血管病临床实践中应用的重要价值及意义,并推荐对大部分疑似或确诊的遗传性心血管病患者进行基因检测,这样不但有助于明确诊断、鉴别诊断、辅助临床诊疗,还可以对高危亲属进行筛查,以便排除患病风险低、无需临床随访的亲属,并帮助鉴别患病风险高的亲属,提早诊断、预防和治疗。另外,检测到明确致病变异后,若有生育健康后代的需求,患者还可以通过产前诊断或植入前遗传学诊断(PGD)进行指导,以减少相应疾病遗传给后代的风险。
部分指南或共识可能会单纯从临床实践的角度或实验室基因检测的角度出发进行推荐,而临床医生和实验室解读人员则可能更多地关注基于自己领域的共识与指南。而我们在日常与临床沟通的过程中,也注意到了临床医生与实验室解读人员之间的部分观点及概念差异。

图1. 欧洲心脏病学会发表的关于心肌病遗传变异的解读及可干预性的立场声明
这在主要由各国临床专家组成的欧洲心脏病学会(ESC)此前在欧洲心脏病杂志(EHJ)上发表的关于心肌病遗传变异的解读及可干预性的立场声明(图1,下文简称为声明)中得到了很好地说明,从基因检测解读实验室的角度看,声明中一些针对变异解读的观点和概念可能会导致误解。因此,安智因生物医学部负责人马懿,联合阜外医院实验诊断中心项目负责人杨航博士,以及华中科技大学同济医学院附属同济医院心血管内科的副主任医师李宗哲博士在EHJ上共同发表了名为“A laboratory viewpoint of the consensus paper from the European Society of Cardiology regarding the utilization of the American College of Medical Genetics and Genomics pathogenic criteria for cardiomyopathy”的文章,旨在从临床实验室的角度针对声明中变异解读的一些可能引起误会的美国医学遗传学与基因组学学会(ACMG)规则进行讨论。
文章内容
ESC最近发表的关于心肌病遗传变异的解读及可干预性的立场声明强调了临床参与在致病性解读中的重要作用,这对临床和实验室团队未来的遗传学研究都有很大的指导意义。然而,从我们实验室的角度来看,对于一些ACMG标准的使用可能考虑得不够全面,容易导致一些误解。
关于PM6的使用
声明建议即使无症状父母一方无法进行检测,也适用中等致病性证据PM6(假定为新发)。如图2和图3所示,该声明建议即使只有无症状父母一方的变异呈阴性,而无症状父母另一方无法进行检测(如已故),也应使用PM6,可假定为新发。然而,假定为新发指的是假定身份为亲生父母,而不是假定为新发的状况。根据ACMG/ClinGen建议和临床指南,必须先对父母双方样本进行检测,且结果均为阴性,才能考虑为新发变异。但事实上,大多数心肌病具有外显率不完全及与年龄相关的差异性表现度。在我们的日常临床检测中,观察到基因型阳性-表型阴性家族成员(甚至在其60多岁时)的情况并不少见(图4)。因此,假定所有已故的无症状父母都是非携带者并应用PM6是不合适的。
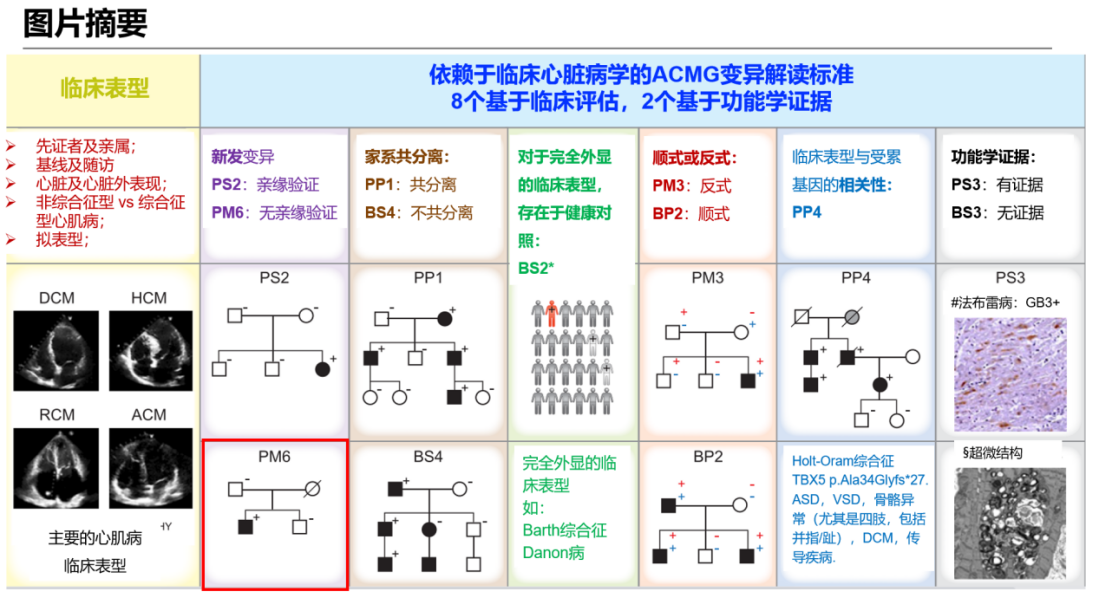
图2. 声明中的图片摘要。(红色方框内的是PM6标准)

图3. 声明中解读标准PM6的详细介绍

图4. 美国医学遗传学和基因组学学会(ACMG)致病标准PM6的不当使用示例。
注:当无症状父母一方不能进行DNA检测时,有两种可能性。在大多数心肌病病例中,可能性1更常见,此时无法假定为新发,因此PM6不适用。
关于PP2的使用
此外,针对心肌病,此声明似乎对于支持性致病性证据PP2可能存在过度使用的嫌疑。根据ACMG指南,PP2应仅适用于良性错义突变发生率低以及致病性错义突变为常见致病机制的基因中发现的错义突变。ClinGen工作组建议考虑将PP2应用于ExAC或gnomAD数据库中针对错义变异z评分>3.095的基因(评分越高表示相应基因转录本更为保守,发生错义变异后致病的可能性越大)。然而,大多数心肌病基因(如MYL2、LMNA、TNNT2和DES)的z评分都低于3.09,良性错义突变并不罕见(图5)。即使对于z评分为3.93的MYH7,ClinGen发布的针对肥厚型心肌病相关MYH7的特异性解读规则中也不推荐使用PP2,因为良性错义突变仅在关键功能域(头部区域,氨基酸181-937)内罕见,而此区域内的变异已经使用重要功能域的中等致病性证据PM1,因此不再适合使用PP2。但如图6所示,PP2在声明中被应用于MYH7p.Arg1250Gly和p.Lys1459Asn,即头部结构域以外的变异。另外,PP2还被用于其他错义突变是主要致病机制,但良性错义突变并不罕见的心肌病致病基因(包括MYL2、LMNA、TNNT2和DES,见图8)。因此,在声明中PP2的应用有些过于宽松,这可能会导致对致病性的高估。
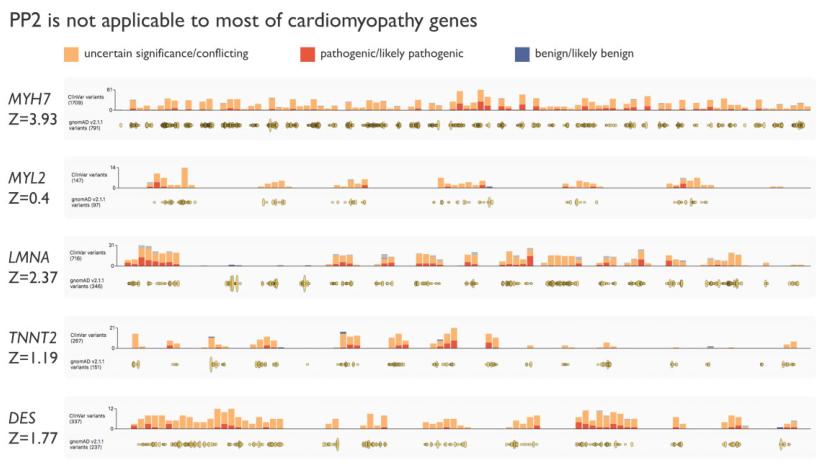
图5. 美国医学遗传学和基因组学学会(ACMG)致病标准PP2的不当使用示例。
注:根据gnomAD数据库(https://gnomad.broadinstitute.org/)中观察到的/预期的错义变异计算的Z分值(Z),分值越大(如>3.09),说明转录本越保守,发生变异更可能致病。gnomAD中记录的错义/框内插入缺失变异(下组)以及ClinVar中致病性/可能致病性(红色)、临床意义未明/冲突的(橙色)和良性/可能良性(蓝色)变异(上组)的数量,也表明了所有基因中良性错义变异相对频繁。该数据来自ClinVar于2022年1月4日发布的数据,图片改编自gnomAD数据库。

图6. 声明中对MYH7头部结构域以外的错义变异使用了PP2。
不使用PP2和PP5将改变声明中一些基因变异的致病性等级
如声明所述,由于各种原因(包括对主要证据的重复使用),ClinGen建议删除支持性致病证据PP5和良性证据BP6(图7)。事实上,如果不使用PP2和PP5这两个支持性证据,声明中引用的许多变异的原致病性将从可能致病(LP)降为临床意义未明的变异(VUS)(图8)。在这种情况下,获取额外的家系样本和完整的临床信息将是提高致病性的最快捷、最简便的方法。

图7. 声明中解读标准PP5和BP6的详细介绍
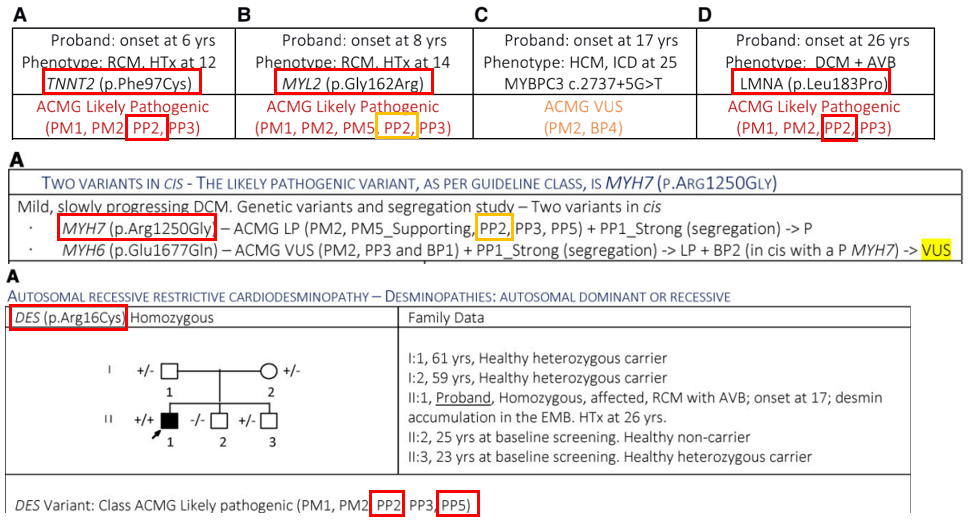
图8. 声明中的PP2、PP5使用示例。
注:如果不使用红色方框内的PP2和PP5支持性致病证据,相应的基因变异的致病性从一开始就达不到可能致病(LP),只能是临床意义未明(VUS),对于后续的临床指导暂时无明确意义。此前补充更多的临床信息和样本验证就会成为提升位点致病性、得到阳性报告的最快捷便利的途径。
总结
对于遗传性心血管病、尤其是心肌病的临床基因检测,在变异解读的过程中应用ACMG致病性判断规则时,可能都要略微谨慎一些,因为过高估计变异位点的致病性最终可能会导致不正确的临床决策。对于携带VUS的患者,如果这些VUS变异高度怀疑是致病性的,但仍然缺乏一些致病性证据(如一个或两个支持标准的证据)来达到可能致病性的分类,此时,定期的临床随访和在其他有类似症状的家族成员中进行VUS变异筛查可能是有助于提高致病性的最为快捷便利的途径。因此,正确的基因检测报告需要临床医生与实验室之间的密切沟通才可能实现。
作者的话
一直以来,临床医生对于基因检测阳性报告的渴望与实验室解读人员对于变异致病性判读的谨慎性之间就存在一定的意见差异。
与无法给予临床任何指导意义的临床意义未明变异(VUS)相比,临床老师可能更希望看到更多的(可能)致病性变异,也因此希望使用更为宽松的致病性判读规则将暂时还缺少一点致病性证据(如一个或两个支持性致病证据)才能达到可能致病的VUS,通过增加一些可能目前不太适合使用或不太推荐使用的证据直接升为可能致病,如目前推荐放弃使用的PP5(其他权威实验室认为该变异致病但无具体证据)和很多基因都不适合使用的PP2(基因上良性变异罕见且错义变异为主要致病方式的新错义变异)。但这样做实际上可能面临风险,毕竟,过高地估计变异位点的致病性最终可能会导致不太正确的临床决策,包括治疗方案及优生优育的选择,从而引起纠纷。
对于临床实验室来说,在遗传性心血管病、尤其是心肌病的变异解读过程中应用ACMG致病性判断规则时,可能都要略微谨慎一些,毕竟这些疾病大多具有外显率不全、表现度差异大、且遗传异质性等特点。因此,除了依赖国际普遍接受的ACMG基本解读规则及ClinGen提出的基因或疾病特异性解读规则外,临床实验室也应综合考虑到基因自身的特点、疾病的临床及遗传特征(外显率及表现度)及此前的自身经验及内部数据库积累,针对某些基因及疾病适当地进行规则的调整。
而对于致病可能性比较大的VUS位点,临床实验室应该更加积极地与临床老师进行沟通,尽可能地通过后续定期的临床随访和在其他有类似症状的家族成员或亲生父母中进行VUS变异筛查来帮助提高位点的致病性(如变异与患病家系成员间存在共分离,或无家族史患者携带的与疾病相关的新发变异等),这也是目前临床基因检测中最为快捷和便利的帮助提高报告阳性率的途径。同时,临床实验室也应对最新文献进行追踪,同时定期对此前数据进行再分析,以便发现更多科技发展带来的新致病证据,从而使此前的报告更为精准。
安智因生物医学部的全体解读人员一直以来也是秉持着上述原则,积极与临床医生沟通,定期进行文献更新与数据再分析,希望能够为临床及患者都提供更为精准的基因检测报告与遗传咨询。
参考文献
1. Ma Y, Yang H, Li Z. Eur Heart J. 2022 May 22:ehac263.
2. Arbustini E, Behr ER, et al. Eur Heart J. 2022 May 21;43(20):1901-1916.
3. Richards S, Aziz N, Bale S, et al. Genet Med 2015;17:405–424.
4. Kelly MA, Caleshu C, Morales A, et al. Genet Med 2018;20:351–359.
5. Ommen SR, Mital S, Burke MA,et al.Circulation 2020;142:e558–e631.
编辑/审校:赵燕檬(市场部)