

抗血小板药物——氯吡格雷
急性冠脉综合征(acute coronary syndrome, ACS)患者经皮冠状动脉介入治疗(percutaneous coronary intervention, PCI)后,血栓事件复发的风险很高。动脉血栓形成的基础涉及血小板的活化和聚集。因此,抗血小板治疗对于预防PCI术后血栓事件的发生至关重要。阿司匹林联合P2Y12受体拮抗剂(如氯吡格雷或替格瑞洛),是PCI术后患者接受抗血小板治疗的基本和常规的用药方案,可以降低血栓形成的风险。大多数指南推荐替格瑞洛作为首选,当替格瑞洛不可用时推荐氯吡格雷。然而,在临床上,由于替格瑞洛的禁忌症、副作用或其他临床因素,首选的抗血小板药物还是氯吡格雷。
氯吡格雷只有在体内被药物代谢酶(如CYP2C19)代谢成活性代谢产物后,才能抑制血小板聚集,但个体差异较大。一部分患者在抗血小板治疗期间会出现残留的高血小板反应性(high platelet reactivity, HPR),而HPR与血栓形成事件显著相关。使用抗血小板药物治疗后出现HPR残留的主要影响因素之一是CYP2C19基因多态性,可以影响氯吡格雷代谢过程。CYP2C19功能丧失(loss-of-function, LOF)等位基因(CYP2C19 *2和CYP2C19 *3)与氯吡格雷代谢效率低、抗血小板作用降低有关[1]。
药物代谢酶基因——CYP2C19
CYP2C19参与氯吡格雷、S-美芬妥英、奥美拉唑、伏立康唑、安定、去甲安定等药物的代谢。CYP2C19遗传变异可导致酶活性的个体差异,使人群出现超快代谢者(ultrarapid metabolizer,UM)、广泛代谢者(extensive metabolizer,EM)、中间代谢者(intermediate metabolizer,IM)和慢代谢者(poor metabolizer,PM)4种表型。CYP2C19基因多态性的分布存在明显的种族和地区差异。CYP2C19 *2(rs4244285,c.681G>A)和CYP2C19 *3(rs4986893,c.636G>A)是中国人群中存在的2种导致CYP2C19酶缺陷的主要等位基因[2]。CYP2C19 *2等位基因,在白人和黑人人群中占大约15%,在亚洲人群中占29-35%。
基于CYP2C19基因分型的抗血小板个体化治疗对PCI术后患者血小板功能的影响
在以往的临床研究中,基于CYP2C19基因分型确定最佳抗血小板治疗方案方面的结论并不一致。例如,POPular Genetics研究[3](NCT01761786)纳入2488例PCI术后患者,标准治疗组采用指南推荐的替格瑞洛/普拉格雷治疗12个月,基因型指导组中携带CYP2C19 LOF的患者接受替格瑞洛/普拉格雷进行治疗,未携带者接受氯吡格雷治疗。结果显示,与标准治疗组相比,基因型指导组患者PCI术后1年内发生全因死亡、心肌梗死、明确支架内血栓形成、卒中或大出血的风险并未升高(5.1% vs.5.9%,非劣性检验,p<0.001),且基因型指导组比标准治疗组患者的出血风险更低(9.8% vs.12.5%;P = 0.04)。而TAILOR PCI研究[4](NCT01742117)结果显示,与常规治疗组相比,基因型指导组的主要复合终点事件并没有显著降低。
而基于中国人群的研究中,Zhang等[1]纳入了1063例中国ACS患者,在CYP2C19基因分型基础上给予患者抗血小板个体化治疗,并采用血栓弹力图(TEG)评估血小板反应性。根据临床特征,分为传统抗血小板治疗组(CA)和个体化抗血小板治疗组(IA)。IA组中,CYP2C19 EMs占51.0%,IMs占36.4%,PMs占12.6%,这与CYP2C19 *2或CYP2C19 *3等位基因突变率的既往研究报道类似。研究具体结果如下:
(1)IA组MAADP>47 mm(血栓形成高风险)患者的比例(29.6%)明显低于CA组(38.1%)。IA组MAADP≤31 mm(出血高风险)患者比例(31.0%)明显高于CA组(21.3%) (p<0.001)。这些结果提示,IA组ACS患者血栓形成风险较低,但出血风险较高(见图1)。
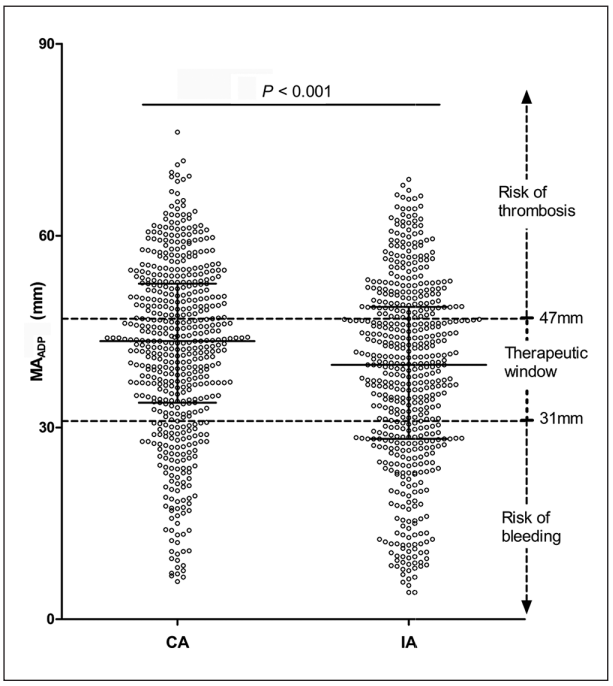
图1 CA组与IA组MAADP值的比较
(2)PMs患者中MAADP>47 mm的比例显著低于EMs组,MAADP≤31 mm的比例显著高于EMs组(p<0.001)。这些结果提示,具有两个LOF等位基因的ACS患者经替格瑞洛治疗后血栓形成的风险较低,但出血的风险较高(见图2)。
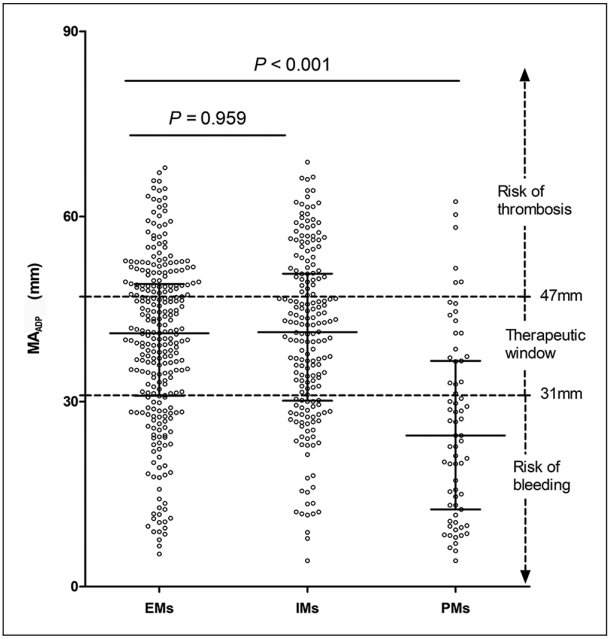
图2 IA组三种代谢类型MAADP值的比较
综上所述,与常规疗法相比,基于CYP2C19基因分型的抗血小板个体化治疗可降低PCI术后ACS患者HPR的发生率。因此,通过服用双倍剂量的氯吡格雷,CYP2C19 LOF等位基因患者可以克服氯吡格雷与LOF等位基因相关联的功能降低而又不增加出血风险,这对于PCI术后ACS患者抗血小板治疗的管理具有指导意义。
氯吡格雷个体化用药基因检测
氯吡格雷是一种前体药物,只有通过机体代谢才会产生具有活性的抗血小板代谢产物,而位于肝脏中的CYP2C19酶在其代谢过程中起重要作用。CYP2C19的不同基因型影响其编码酶的活性及氯吡格雷的代谢速率,进而影响疗效及副作用。
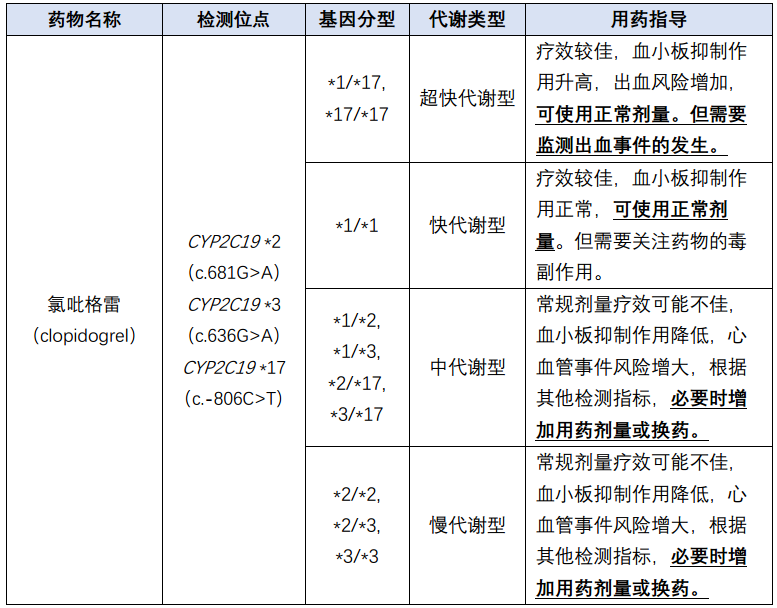
检测内容如下表:
参考文献:
[1] Min Zhang, et al. (2020). Effects of individualized antiplatelet therapy, based on CYP2C19 genotyping, on platelet function in patients underwent percutaneous coronary intervention. Perfusion.
[2] 药物代谢酶和药物作用靶点基因检测技术指南(试行). 2015.
[3] Claassens, D.M.F., et al. (2019). A Genotype-Guided Strategy for Oral P2Y12 Inhibitors in Primary PCI. N. Engl. J. Med. 381, 1621–1631.
[4] Pereira, N.L., et al. (2020). Effect of Genotype-Guided Oral P2Y12 Inhibitor Selection versus Conventional Clopidogrel Therapy on Ischemic Outcomes after Percutaneous Coronary Intervention: The TAILOR-PCI Randomized Clinical Trial. JAMA 324, 761–771.
[5] https://www.pharmgkb.org/.
往期回顾:
精准用药专栏│他汀类降脂药的个体化治疗