


近期,在《Nature Reviews Cardiology》上发表了题为“Pathophysiology and risk factors of peripartum cardiomyopathy”的研究论文,该论文综述了围产期心肌病(PPCM)的基本病理生理机制和危险因子的最新研究。
摘要
围产期心肌病(PPCM)是一种潜在致命的特发性心力衰竭,在不同国家和种族群体中患病率不同。PPCM的病因尚不清楚,但环境和遗传因素以及妊娠相关条件,如先兆子痫,都能导致PPCM的发生。此外,动物研究表明,血管和代谢功能受损可能是PPCM发展的关键。有必要更好地理解参与PPCM发展的致病机制,以建立可以改善PPCM患者结局的新疗法。妊娠激素严格控制着母体的大量适应性反应,包括心血管系统的血液动力学、结构和代谢变化。PPCM患者的围产期与剧烈而快速的激素波动有关,这会导致短暂的心血管(代谢)稳态紊乱,容易出现继发性干扰。本文综述了PPCM的基本病理生理机制和危险因子的最新研究,着重讨论了与妊娠相关的母体心血管变化。作者提供了一个更新的框架来进一步理解PPCM的发病机制,这可能会改进疾病的定义。
要点
妊娠期心血管的生理变化介导了易患围产期心肌病(PPCM)女性的疾病发展。
PPCM的危险因子包括在其他类型心肌病中常见的遗传变异,先兆子痫和癌症史等。
PPCM的发病通常与妊娠晚期和分娩时激素水平的极端波动重叠。
PPCM小鼠模型研究表明,该疾病是由代谢途径失调和血管生成失衡引起的,可能是激素信号异常所致。
我们对PPCM基础病理生理学的理解主要来源于动物模型的研究,这需要在患者研究中得到证实,但这些临床前数据构成了当前临床指南和未来实验的基础。
激素对心血管的影响
性相关和妊娠相关激素是妊娠各个阶段的关键调节因子。包括雌激素和黄体酮在内的几种激素会对心血管系统产生深远影响,但鉴于大多数研究都是在动物模型中进行的,这些影响在人体中的具体分子机制在很大程度上还不清楚(图1)。
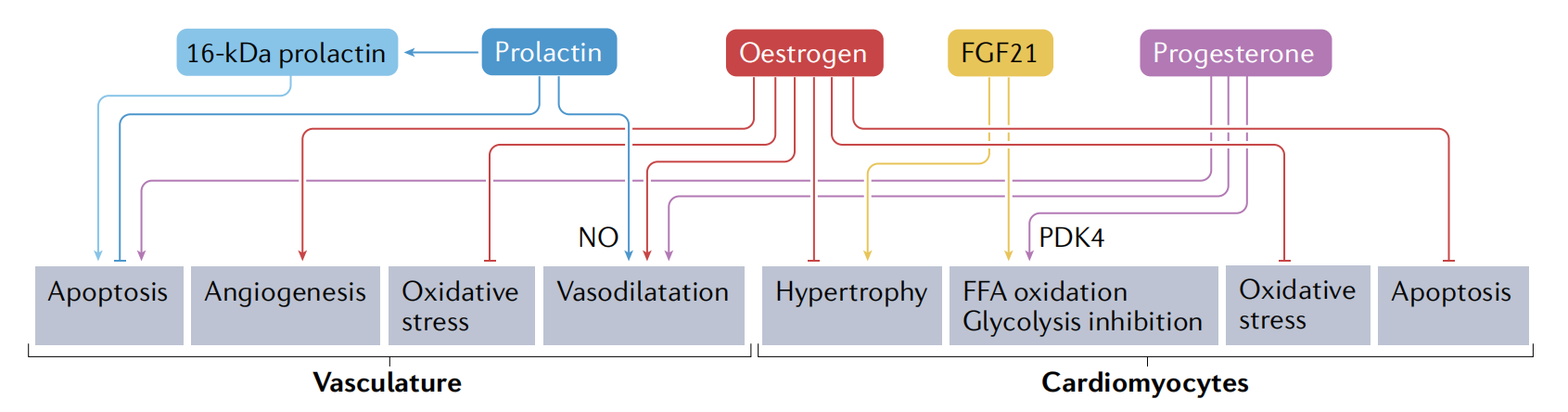
图1. 妊娠激素引起心血管特异性效应
注:妊娠激素催乳素(及其裂解产物16-kDa催乳素)、雌激素、成纤维细胞生长因子21(FGF21)和黄体酮在血管系统和心肌细胞中有多效性作用,包括促进或抑制凋亡、血管生成、代谢信号、血管舒张、心肌肥厚和氧化应激。FFA,游离脂肪酸;NO,一氧化氮;PDK4,丙酮酸脱氢酶激酶4。
PPCM的生物标记物和危险因素
尽管PPCM的确切病因目前尚不清楚,但已经提出了几个风险因素,包括心力衰竭相关的遗传缺陷、种族、高血压疾病、感染、双胞胎和后续妊娠以及癌症史。
遗传:
鉴于PPCM和DCM具有相似的临床特征,PPCM被认为是DCM(扩张型心肌病)疾病谱的一部分。一些诊断为PPCM的患者可能之前有未被识别的DCM,尽管在临床诊断为PPCM之前偶然获得超声心动图的少数病例中,LVEF(左心室射血分数)正常。遗传学研究表明,BAG3(编码BAG家族分子伴侣调节因子3)、DSP(编码桥粒斑蛋白)、FLNC(编码细丝蛋白C)、LMNA(编码核纤层蛋白A/C)、MYH6和MYH7(分别编码肌球蛋白6和肌球蛋白7)、TNNC1(编码心肌和骨骼肌的慢型肌钙蛋白C)、TTN(编码肌联蛋白)和VCL(编码黏着斑蛋白)的变异在PPCM和DCM患者中都被发现。具体而言,在大约10%的PPCM患者中发现了TTN的截短变异(DCM最常见的遗传原因)。此外,在PPCM患者中发现这些基因变异的频率与扩张型心肌病患者的频率相似,这强调了这两种疾病的遗传易感性的相似性。BAG3变异与PPCM的关联也促使人们提出了一个假说,即不同种类的分子伴侣(如热休克蛋白)可能参与PPCM的发病机制。一项小规模全基因组关联分析在79例PPCM患者中发现了PTHLH(编码甲状旁腺激素相关蛋白)附近的单核苷酸多态性富集,但这需要进一步研究才能与PPCM发病机制联系起来。事实上,PPCM和DCM可能是由类似的基因变异引起的,其中TTN中的变异似乎最为普遍。然而,这些变异是如何聚合导致PPCM的,仍有待研究。
PPCM的病理生理学
关于人类PPCM的病理生理学知之甚少。上述危险因素为PPCM患者在诊断时和不同随访期的状况提供了一些见解,但这些数据并不支持最终导致PPCM的病理机制的相关推论。到目前为止,现有的数据主要是通过动物模型获得的,这些动物模型的疾病表型类似于人类的PPCM。尽管这些动物模型有助于形成一些关于发病机制的临床指南和假设,但大多数假定的机制仍有待在人类中得到证实。
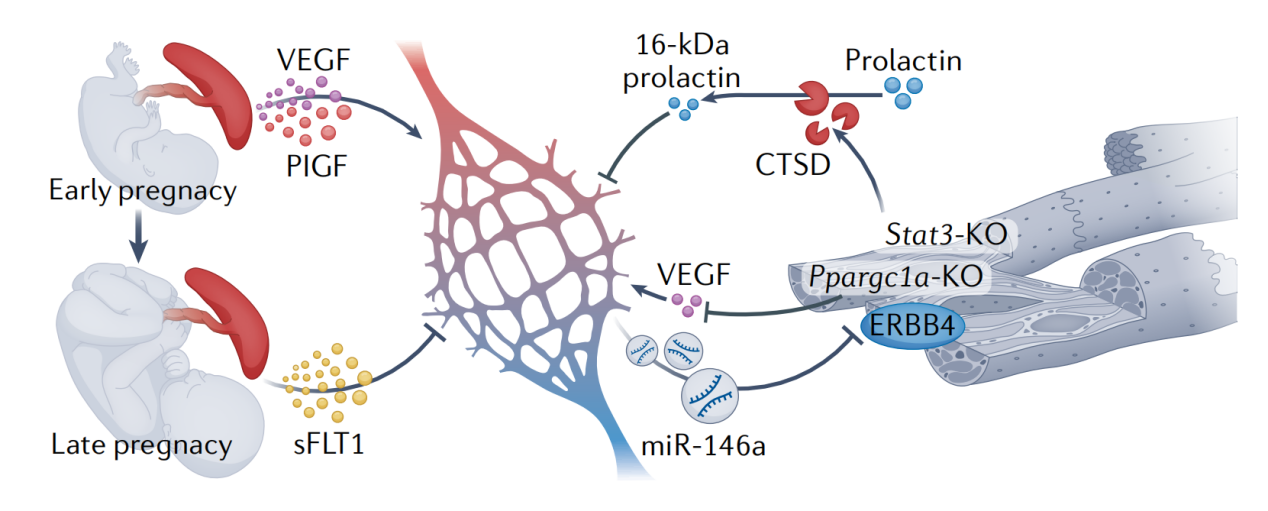
图2. 围产期心肌病的致病途径
注:在妊娠早期,胎盘分泌高水平的血管内皮生长因子(VEGF)和胎盘生长因子(PlGF)进入母体循环,刺激血管生成和器官灌注。随着妊娠的进展,循环中的VEGF和PlGF水平随着抑制血管生成的可溶性fms样酪氨酸激酶1 (sFLT1)分泌的增加而升高。另外,心肌细胞应激诱导蛋白水解酶组织蛋白酶D (CTSD)的胞外分泌,它将催乳素切割成一个对内皮细胞具有细胞毒性的16-kDa片段。因此,内皮细胞分泌载有microRNA-146a (miR-146a)的外泌体,抑制各种心肌细胞进程,包括受体酪氨酸蛋白激酶ERBB4介导的代谢。这两种机制在心脏中都有核心作用,并可能有助于围产期心肌病的发展。值得注意的是,心脏特异性敲除(KO)Stat3或Ppargc1a的小鼠会发生围产期心肌病。
总结
PPCM是一种复杂的疾病,有许多危险因素和病因。鉴于对人类PPCM的发病机制知之甚少,因此PPCM的诊断很困难,建议早期进行有针对性的筛查。广泛的队列研究,如ESC EORP PPCM登记,对提高我们理解PPCM的临床表现、危险因素和预后至关重要。此外,对过去十年来易患PPCM女性遗传因素的深入研究表明,有心肌病家族史的患者进行遗传评估可能是明智的。重要的是,与产后早期相比,妊娠晚期心血管系统发生了根本上不同的变化,而PPCM的根本原因可能与这些阶段发生的变化或分娩引起的转变有关。从机理角度来看,PPCM似乎是由继发于血管功能障碍的心力衰竭引起的。对两种PPCM小鼠模型的研究表明,围产期的血管生成受到严格调控,对有害刺激敏感。来自这些动物模型的数据构成了几个临床研究和建议的基础,尽管对如何将这些临床前研究的观察外推到患者身上的了解还很少。因此,需要对PPCM患者进行机理研究,以进一步了解PPCM的病理生理学。作者所在的研究小组发现,来自PPCM患者的hiPSC-CMs在体外显示出代谢障碍。妊娠激素在妊娠期间和妊娠之后调节了母体的新陈代谢和血管生成。综上所述,妊娠激素可能是PPCM患者心脏中微妙平衡血管生成状态和潜在不稳定代谢过程之间的联系。
参考文献
Hoes MF, Arany Z, Bauersachs J, Hilfiker-Kleiner D, Petrie MC, Sliwa K, van der Meer P. Pathophysiology and risk factors of peripartum cardiomyopathy. Nat Rev Cardiol. 2022 Jan 11. doi: 10.1038/s41569-021-00664-8.
关于肥厚型心肌病及相关内容的更多介绍,如下:
《AHA/ACC肥厚型心肌病的诊断和治疗指南2020年更新》