

背景介绍:扩张型心肌病(DCM)是一种在无冠状动脉疾病或负荷异常情况下,以左心室扩张和收缩功能障碍为特征的心肌病。已报道有50多个基因与DCM相关,该病主要为常染色体显性遗传,且外显率不全。
近日,在《European Heart Journal》上刊登了一篇名为“Genome wide association analysis in dilated cardiomyopathy reveals two new key players in systolic heart failure on chromosome 3p25.1 and 22q11.23”的文章,有助于更好地理解DCM的遗传结构,并揭示心脏衰竭新的生物学途径。
研究方法
在扩张型心肌病中进行了迄今为止最大的全基因组关联研究,在发现队列中有2719名受累个体和4440名健康对照,复制队列中有584例受累个体和963例健康对照。全文摘要概述可参考图1;
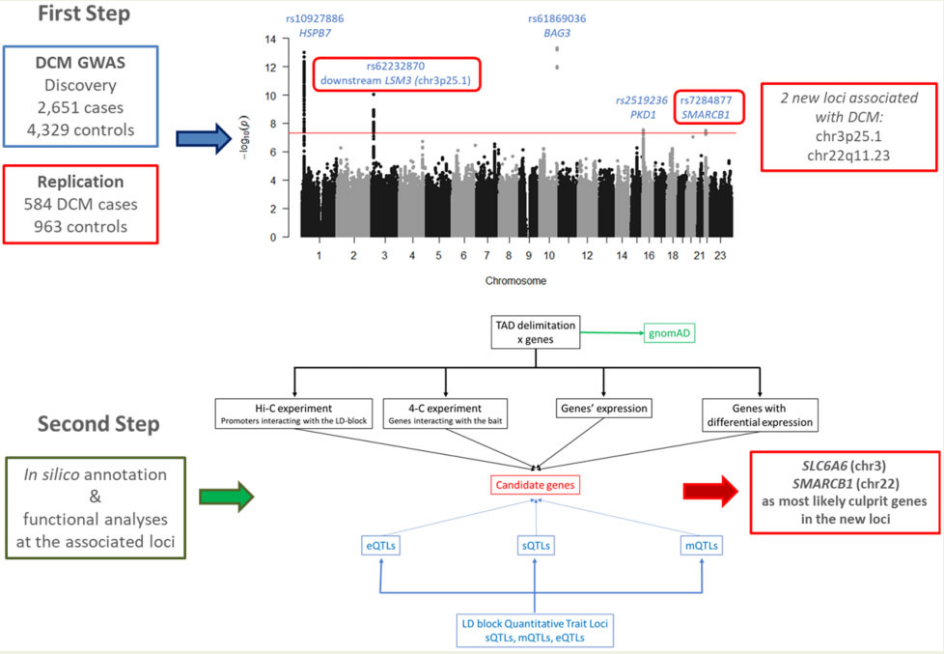
图1 图文摘要。第一步:通过迄今为止对扩张型心肌病进行的最大的全基因组关联研究,在染色体3p25.1和22q11.23上鉴定并重复了两个新的位点;第二步:结合相关位点的硅和功能分析揭漏了每个位点上的最有可能致病基因:SLC6A6(3号染色体)和SMARCB1(22号染色体)。这两个新角色的发现揭示了新的生物学途径和假定的新的治疗靶点。
研究结果
确定了与扩张型心肌病相关的四个位点。其中,位于10号染色体的BAG3 rs61869036 和1号染色体的HSPB7 rs10927886是已知的。鉴定和重复了两个新的相关位点:位于3p25.1号染色体[单核苷酸多态性(SNP)位点rs62232870,分别在发现和重复队列中P=8.7×10-11和7.7×10-4)]和22q11.23号染色体[(SNP 位点 rs7284877,分别在发现和重复队列中P=3.3×10-8和1.4×10-3)]。
根据这四个扩张型心肌病基因座的风险等位基因数构建的遗传风险评分显示,与具有5个风险等位基因的个体相比,具有8个风险等位基因的个体患扩张型心肌病的风险增加了27%,具有1种风险等位基因的个体换扩张型心肌病的风险降低了21%。
iPSC衍生心肌细胞的硅注释和功能4C测序分析表明,在3p25.1染色体上SLC6A6基因最可能导致DCM。该基因编码牛磺酸转运体,其参与心肌功能障碍和DCM,并在人类和动物身上的大量观察结果支持了这一观点。
在22q11.23位点,在硅片和数据挖掘注释中,以及在较小程度上的功能分析,强烈建议SMARCB1基因作为候选致病基因。
小结:迄今为止对DCM进行的最大的全基因组关联研究揭示了3p25.1和22q11.23染色体上两个新的DCM相关位点(在两个位点中最有可能的致病候选基因分别是SLC6A6和SMARCB1),并构建一个多基因风险评分来更好地预测DCM的风险。这项研究为DCM的遗传结构提供了更好的理解,鉴定了与收缩性心力衰竭病理生理学的新参与者,具有新的治疗发展潜力。
更多心肌病相关信息,详见: